Правда и вымысел вокруг иммунотерапии. Интервью с онкологом Михаилом Ласковым
09.11.2018
В октябре Нобелевку вручили исследователям иммуотерапии. Если и раньше вокруг этого метода ходило много слухов, то после решения Нобелевского комитета ажиотаж возрос еще больше. Мы поговорили с онкологом Михаилом Ласковым о том, что такое иммунотерапия и что выдают за иммунотерапию, при лечении каких видов рака она наиболее эффективна, и почему во многих случаях ее нельзя использовать.
- Обновление. В сентябре 2022 года мы опубликовали новый материал об иммунотерапии онкологических заболеваний. В нем подробно рассказываем, как работают иммуноонкологические препараты и в каких ситуациях они могут назначаться, как проводится иммунотерапия и какие побочные эффекты возникают чаще всего. Прочитать статью можно по этой ссылке.
Что такое иммунотерапия?
Иммунотерапия – это относительно новый метод лечения онкологических заболеваний. Иммунотерапия не действует напрямую на опухоль, но заставляет иммунитет убивать раковые клетки. Это и есть принципиальное ее отличие от химиотерапии и таргетной терапии.
По большому счету, иммунотерапия заставляет иммунитет делать то, что он и так должен, но не делает по каким-либо причинам. Например, иногда раковые клетки маскируются под здоровые, тогда иммунная система перестает воспринимать их как инородные и не уничтожает. Иммунотерапия может “снимать маску” с опухолевых клеток и помогать иммунитету распознавать их.
Справедливости ради нужно сказать, что сейчас поднялся очень большой хайп по поводу иммунотерапии, потому что вышли действительно эффективные препараты: авелумаб, атезолизумаб, дурвалумаб, пембролизумаб, ниволумаб и ипилимумаб. Но иммунотерапия началась, конечно же, не сейчас и даже не три года назад. Она очень давно применялась с переменным успехом. Как правило, с не очень большим.
Что же произошло сейчас? Появился новый класс препаратов, которые действуют на рецепторы PD1 и PD-L1. Именно эти рецепторы позволяют опухолевой клетке повлиять на иммунитет так, чтобы он перестал распознавать ее, и, следовательно, убивать раковые клетки.
Для лечения каких видов рака используется иммунотерапия?
Сначала эти препараты начали применяться при меланоме и имели большой успех. Почему именно при меланоме? Как мы понимаем, есть опухоли, которые лечатся относительно легко, а есть те, что лечатся очень плохо, рак поджелудочной, например.
Новые препараты стараются разрабатывать именно для труднолечимых раков. Меланома – это как раз один из таких труднолечимых раков, в лечении которого двадцать лет не происходило ничего хорошего, никаких новых высокоэффективных препаратов не появлялось.
Иммунотерапия показала себя очень эффективно при меланоме, все воодушевились и начали применять этот метод лечения на все раки, которые только могли. Тут, конечно же, очень быстро выяснилось, что где-то он работает, где-то не работает совсем, а где-то работает только в конкретных ситуациях.
Иммунотерапия сейчас успешно применяется при лечении рака легких. Как мы знаем, есть разные мутации и разные виды этого рака. И при некоторых из них иммунотерапия быстро заменила химию, оказалась и лучше, и безопаснее. Это очень большой успех. Но стоит помнить, что далеко не весь рак легких успешно лечится иммунотерапией.
В России иммунотерапию также используют при лечении рака почек, а на Западе – в случаях рака головы и шеи, лимфомы Ходжкина, рака мочевого пузыря и некоторых случаях рака печени.
Как объяснить, что иммунотерапия подходит только по показаниям и небольшому проценту больных?
Как и все, что есть в онкологии, иммунотерапия – это не панацея от всего рака. Это просто еще один способ воздействовать на опухоль, далеко не всегда эффективный и ни разу не безопасный
Использовать иммунотерапию можно лишь в ограниченном количестве случаев. На данный момент ее эффективность доказана только для следующих видов рака:
— меланома;
— немелкоклеточный рак легких;
— мелкоклеточный рак легких;
— рак почки;
— рак головы и шеи;
— лимфома Ходжкина;
— рак мочевого пузыря.
*** Иммунотерапия может быть эффективной в строго определенных ситуациях даже при вышеуказанных видах рака.
К тому же есть ряд побочных эффектов. И довольно серьезных. В некоторых случаях иммунная система начинает атаковать здоровые ткани и органы, что может вызвать такие осложнения, как:
— пневмония,
— гормональные нарушения,
— проблемы с желудочно-кишечным трактом,
— нефрит и нарушение функции почек,
— мышечные боли, боли в костях и суставах,
— ощущение усталости, слабость,
— тошнота, диарея, нарушения аппетита и др.
Впрочем, серьезные осложнения появляются в среднем только в одном случае из шести.
В октябре вы назвали Нобелевскую премию за иммунотерапию премией для маркетологов. Почему вы отреагировали именно так?
Вспомним историю прекрасного препарата бевацизумаб. Когда он вышел, маркетологи подняли хайп по поводу этого средства, которое останавливает рост сосудов в опухоли. Начали из каждого утюга говорить о том, какое это чудо-чудо-чудо. В итоге, конечно, никакого чуда не было, и этот препарат нашел свое довольно ограниченное применение. И по соотношению цена-польза он, вежливо говоря, далеко не идеален.
И вот уже на этой неделе ко мне толпами приходят люди, которые пытаются спастись при помощи иммунотерапии. И только максимум у 10 % из них этот метод можно пробовать с неизвестным результатом.
Вот про такую ситуацию как раз и было предостережение в этом посте. Потому что на этом сейчас можно быстро срубить много денег в России, именно срубить, а не заработать. Ведь у людей есть все подтверждения: 1) не могли просто так дать Нобелевку; 2) все журналисты написали, что это чудо и панацея; 3) препарат стоит от 200 тысяч в месяц. Все сходится – Нобелевка, цена. Отлично, квартиру продаем.
И тут еще какой-нибудь радостный доктор из частной клиники предлагает его назначить и прямо сейчас, ведь завтра может быть уже поздно.
И главное – очень хочется верить, что это спасет. Это ведь не гомеопатия, а высокая наука.
Как пациенту понять, назначают ему фейковые препараты или нормальные?
Это сделать можно, но необходимо, конечно, включать голову. Нужно много читать и стараться уметь разбираться в источниках.
Например, почитать гайдланы для пациентов NCCN или ESMO. Это англоязычные источники, NCCN – американский , ESMO – европейский. Кстати, мы сейчас переводим их на русский язык при помощи благотворительного фонда «Живой».
Еще можно посмотреть русскоязычные рекомендации, но только профессиональные.
Тут проблема, конечно, в том, что на русском языке практически ничего нету. Существуют клинические рекомендации, но они для врачей. Для пациентов – почти ничего. Вот у нас (на ютуб-канале Клиники амбулаторной онкологии и гематологии — примечание Profilaktika.Media) есть видео про иммунотерапию. Еще пара моих комментариев и несколько материалов моих коллег на эту тему. Но в общем море «ура-ура, нашли лекарство от рака», «британские ученые доказали…» это может быть очень сложно найти.
А какие препараты иммунотерапии используются сейчас в России?
Их всего четыре, и они довольно дорогие. Это атезолизумаб «Тецентрик», пембролизумаб «Кейтруда», ипилимумаб «Ервой» и ниволумаб «Опдиво». И все, больше пока ничего нет, но много всего на предрегистрационной стадии.
Какие “методики” на рынке выдают за фальшивую иммунотерапию? Например, назначают профилактические капельницы с иммуномодуляторами против рака.
Инарон, рефнот, вакцины всякие, фракция АСД, всего и не упомнишь.
Как пациенту понять, что ему нужна и может помочь иммунотерапия и как ее можно попробовать получить в рамках ОМС?
Поговорить с врачом, почитать надежные источники (об этом выше). По ОМС пойти к химиотерапевту по месту жительства. Все, больше никак.
За счет чего иммунотерапия такая дорогая? Из чего складывается стоимость лекарства?
Разработка нового лекарства, действительно нового, как эти ингибиторы, стоит миллиард долларов. И семь лет после разработки формула защищена патентом. После этого срока буквально на следующий же день заранее скопированный препарат начинают продавать дешевле.
Появляется большая конкуренция. Соответственно, за эти семь лет люди, работающие над созданием лекарства, должны вернуть себе “ярд” и заработать. Один “ярд” что в себя включает? Что из 10 лекарств, которые на ранней стадии компания начинает разрабатывать, до клиник доходит только одно, и это занимает лет двадцать.
Соответственно, вот и вся экономика, за 7 лет нужно всю стоимость отбить и немного заработать для акционеров. Очень сложно разрабатывать и очень просто копировать.
Как пациенту понять, что он наткнулся на мошенников?
Сигнальный значок – это, прежде всего, давление. Когда начинается – давайте скорее, уже вчера надо было начать применять препарат, думать вам некогда, по другим местам ходить нечего. То есть такие довольно простые элементы давления.
В онкологии, на самом деле, крайне редко бывает так, что необходимо вот прямо сейчас, сию минуту начать лечение.
Понятно, что если требуют много денег и есть давление по времени, чтобы человек не успел одуматься, то, скорее всего, что-то не так.
Трекрезан: инструкция по применению
Дата публикации: 25.05.2022
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ВОЗМОЖНЫ ПОБОЧНЫЕ ЭФФЕКТЫ. НЕОБХОДИМА КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА.В сезон простудДля иммунитетаПри простудеСредства от простудыУкрепление иммунитета
Автор статьи
Подойницына Алёна Андреевна
,
Диплом о фармацевтическом образовании: 105924 3510722 рег. номер 31917
Все авторы
Содержание статьи
- Таблетки «Трекрезан» от чего принимают
- «Трекрезан» действующее вещество
- «Трекрезан» противовирусный препарат или нет
- «Трекрезан» принимать до еды или после
- «Трекрезан» совместимость с алкоголем
- «Трекрезан» аналоги
- «Трекрезан» или «Арбидол»: что лучше
- Задайте вопрос эксперту по теме статьи
Кашель, насморк, слабость и ломота во всем теле… Всем известные симптомы острого респираторного заболевания. Всегда заболевание приходит не вовремя и длиться долго, выбивая из колеи любого человека. Чтобы избежать таких неприятных встреч с вирусом стоит заранее подготовить свой иммунитет. Особенно в осенне-весенние периоды, когда наблюдается рост простудных заболеваний.
Расскажем о препарате «Трекрезан», от чего и для чего его применяют, что входит в его состав, как правильно пить таблетки, совместимы ли они с алкоголем и главное не относятся ли они к антибиотикам.
Таблетки «Трекрезан» от чего принимают
Лекарственное средство «Трекрезан» принимают в комплексной терапии:
- при профилактике и лечении острых респираторных вирусных инфекций;
- в период высоких интеллектуальных и тяжелых физических нагрузок;
- для повышения устойчивости организма различным стрессовым воздействиям (гипоксия, перегревание, переохлаждение) и неблагоприятным воздействиям окружающей среды (резкая смена климатических условий, адаптации к перепадам атмосферного давления).
«Трекрезан» действующее вещество
В состав препарата входит:
- действующее вещество — оксиэтиламмония метилфеноксиацетат;
- вспомогательные вещества: лактозы моногидрат (сахар молочный) — 200 мг, крахмал картофельный — 92.5 мг, натрия стеарилфумарат — 5 мг, кремния диоксид коллоидный (аэросил) — 2.5 мг.
«Трекрезан» противовирусный препарат или нет
Нам часто задают вопросы о средстве «Трекрезан»: является ли препарат противовирусным, а антибиотик это или нет.
Лекарственное средство «Трекрезан» не обладает ни противовирусным действием, ни антибактериальным. Его основное действие направлено на иммуностимулирующий эффект. Другими словами — заставляет работать иммунитет человека.
«Трекрезан» принимать до еды или после
Не остается без внимания и вопрос о времени приема таблеток, до еды или после еды. Как указано в инструкции по применению, таблетки «Трекрезан» принимают после еды.
«Трекрезан» совместимость с алкоголем
О возможной совместимости препарата с алкоголем в инструкции производитель не указал информации. Поэтому мы советуем придерживаться общепринятых рекомендаций, и не принимать алкоголь совместно с лекарственными средствами. Так как это может вызвать ослабление терапевтического эффекта.
«Трекрезан» аналоги
Рассматривая препараты-аналоги с одинаковым действующим веществов, то это:
- «Трекрезолид» — полностью аналогичный препарат, отечественного производителя, цена немного ниже чем у «Трекрезан»;
- «Трекресил» — также идентичен в характеристиках препарату «Трекрезан», по стоимости одинаков с «Трекрезолид».
Хотите разбираться в аналогах лекарств, чтобы умело подбирать препараты на свой бюджет? Наша методичка от экспертов-провизоров «Аналоги популярных лекарств» поможет вам в этом! Получить методичку просто: подпишитесь на наши соцсети и напишите в сообщения «аналоги».
Мегаптека в соцсетях: ВКонтакте, Telegram, OK, Viber
«Трекрезан» или «Арбидол»: что лучше
Сравнить и выделить какое из средств лучше не возможно. Причина тому, что действие этих лекарств абсолютно разное, хотя на первый взгляд и не скажешь.
Действие «Трекрезан» заключается в стимулировании собственного иммунитета, то есть препарат относится к иммуномодуляторам. Противовирусного действия у этого лекарства нет.
«Арбидол» в составе которого действующее вещество — умифеновир. Это противовирусный препарат, и он направлен на уничтожение вируса в клетках организма.
Таким образом «Трекрезан» подойдет для комплексного лечения ОРЗ, в то время как «Арбидол» может быть назначен единственным препаратом.
Подведем итоги о препарате «Трекрезан». Это иммуномодулятор, который подходит для профилактики заболеваний. С помощью своего действующего вещества — оксиэтиламмония метилфеноксиацетат, препарат активирует и заставляет работать клетки иммунитета. «Трекрезан» не относится ни к группе противовирусных, ни к группе антибиотиков, он выполняет свою, другую роль в организме человека.
В инструкции производитель указал, что принимать таблетки следует после еды.
У лекарства имеются 2 препарата-аналога, идентичные по характеристикам, так как имеют одинаковый состав действующего вещества.
Выбирая между лекарствами, например между «Арбидол» и «Трекрезан» стоит внимательно читать инструкцию, и обращать внимание на действие лекарства. То есть если вам нужен противовирусный эффект, то стоит выбрать «Арбидол», а если для профилактики — «Трекрезан». А вернее всего не заниматься самолечением и обратиться к врачу за консультацией.
Задайте вопрос эксперту по теме статьи
Остались вопросы? Задайте их в комментариях ниже – наши эксперты ответят вам. Также вы можете поделиться своим опытом с другими читателями Мегасоветов.
Поделиться мегасоветом
Понравилась статья? Расскажите маме, папе, бабушке и тете Гале из третьего подъезда
Цены на товар Трекрезан:
Мегаптека,
Цены на Трекрезан в Санкт-Петербурге, Цены на Трекрезан в Новосибирске, Цены на Трекрезан в Екатеринбурге, Цены на Трекрезан в Казани, Цены на Трекрезан в Нижнем Новгороде, Цены на Трекрезан в Челябинске, Цены на Трекрезан в Самаре, Цены на Трекрезан в Уфе, Цены на Трекрезан в Ростове-на-Дону, Цены на Трекрезан в Омске, Цены на Трекрезан в Красноярске, Цены на Трекрезан в Воронеже, Цены на Трекрезан в Перми, Цены на Трекрезан в Волгограде, Цены на Трекрезан в Краснодаре, Цены на Трекрезан в Тюмени, Цены на Трекрезан в Саратове, Цены на Трекрезан в Тольятти, Цены на Трекрезан в Ижевске, Цены на Трекрезан в Барнауле
Гид по аналогам за подписку
подпишитесь на соцсети и напишите в сообщения «аналоги»
Статья на конкурс «Био/Мол/Текст»: Корректировка диеты часто применяется для лечения и профилактики заболеваний. Онкологические заболевания — не исключение: правильное питание может служить не только профилактической мерой, но и повышать эффективность терапии. Здесь мы предлагаем обсудить «вкусовые предпочтения» раковых клеток и разобраться в том, как отдельные питательные вещества могут помочь бороться с опухолью.
Конкурс «Био/Мол/Текст»-2021/2022
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2021/2022.
Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.
Генеральный партнер конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Введение: на вкус и цвет товарищей нет
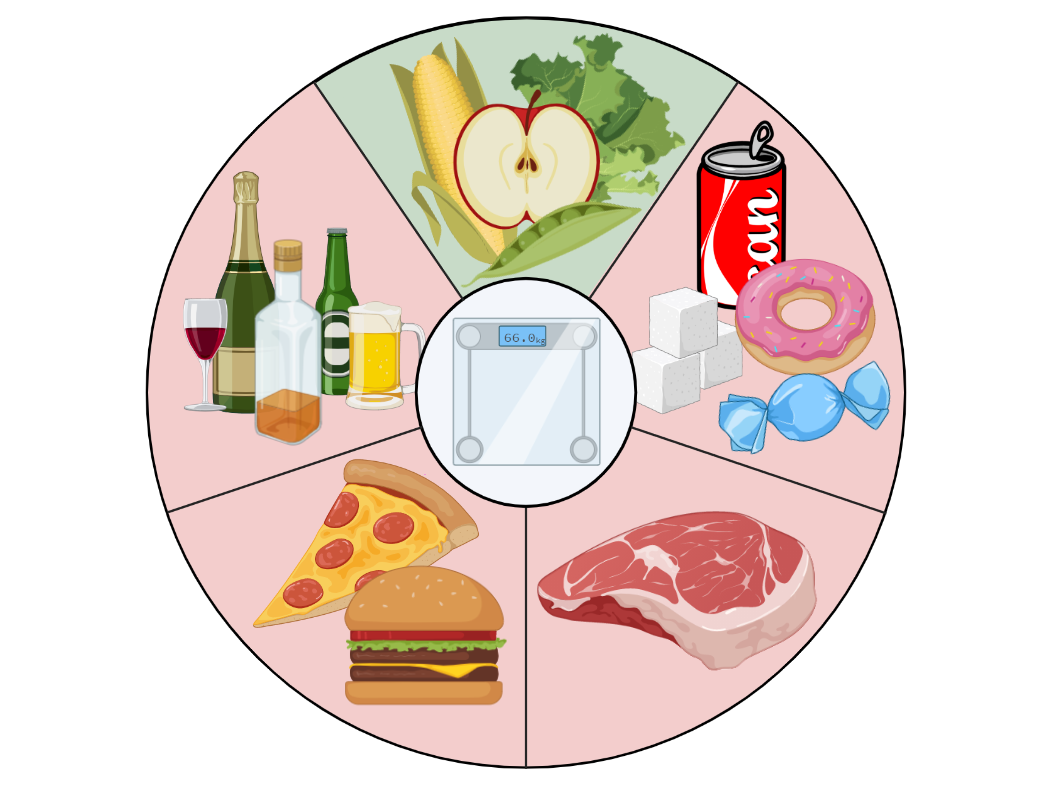
С начала 1980-х годов ведущие организации здравоохранения выпускают рекомендации по питанию и образу жизни, которые позволяют снизить индивидуальный риск развития рака. Данные рекомендации основаны на результатах метаанализов эпидемиологических исследований (иными словами, анализ многолетнего опыта миллионов людей, которые питались тем или иным образом). Эти рекомендации универсальны и просты в исполнении: они не требуют подсчета калорий, строгого контроля состава продуктов, а лишь предлагают общую схему и принцип питания для поддержания здорового веса (рис. 1).
Рисунок 1. Рекомендации по питанию, которые направлены на снижение вероятности возникновения онкологических заболеваний. Ежедневный рацион должен включать фрукты, овощи, бобовые культуры, цельнозерновые крупы. По возможности, необходимо ограничивать употребление красного мяса, сахара, сладких газированных напитков и алкоголя. Следование данным советам позволит поддерживать здоровый вес в течение всей жизни и снизить индивидуальный риск развития рака.
коллаж авторов статьи. Создан с помощью BioRender.com
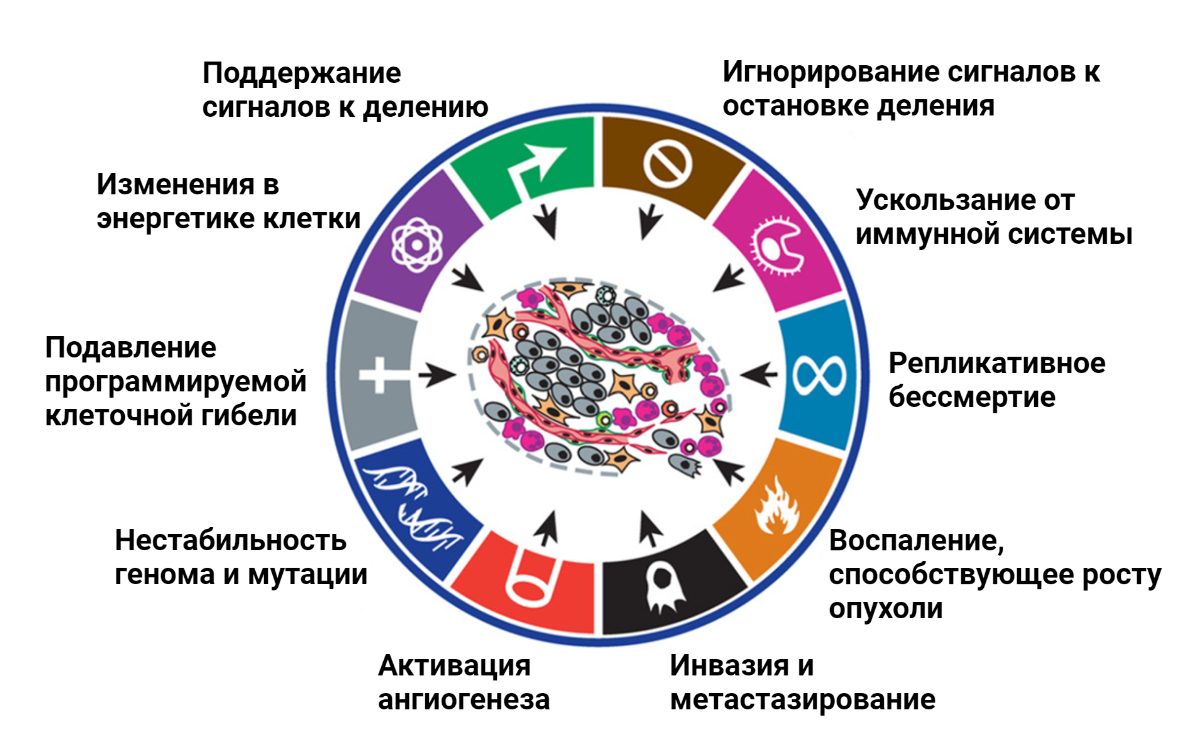
Подобного рода советы относятся к здоровым людям, тогда как для людей, страдающих онкологическими заболеваниями, стандартных рекомендаций по питанию не существует. В то же время, питание пациентов может сильно влиять на успешность терапии злокачественных образований [1]. Почему для людей, больных раком, нельзя составить универсальные рекомендации по составу пищи? Ответ на этот вопрос следует из принципов, согласно которым развиваются все опухоли [2]. Изначально клетка, которая в будущем даст начало опухоли, ничем не отличается от своих соседей. По мере накопления мутаций нормальные клетки могут постепенно эволюционировать и приобретать черты раковых клеток [3], [4]. В 2000 году среди многочисленных особенностей рака, в легендарном обзоре Hallmarks of cancer [3] были обозначены основные признаки, которые определяют биологию опухолевой клетки (рис. 2).
Рисунок 2. Особенности опухолевых клеток (hallmarks of cancer), которые отличают их от нормальных. Были сформулированы в 2000 году [3] и затем дополнены в 2011 [4].
адаптировано из [4]
Важнейшей особенностью всех раковых клеток является нестабильность генома, которая приводит к огромному генетическому разнообразию опухолей. Несмотря на ряд свойств, присущих всем раковым клеткам, каждая опухоль обладает уникальным набором мутаций, которые и определяют ее агрессивность, скорость роста, эффективность терапии. Генетическое разнообразие опухолей является основной преградой для составления универсальных рекомендаций по питанию для пациентов.
В последнее время исследователи активно изучают влияние питательных веществ на прогрессию опухоли и эффективность лечения. В основном проводятся экспериментальные работы на животных моделях, но есть и немногочисленные клинические исследования. Мы предлагаем читателям познакомиться поближе с особенностями метаболизма опухолевой клетки. Попытаемся разобраться, как вещества, потребляемые с пищей, могут влиять на опухоль и ее окружение. И, наконец, попробуем ответить на вопрос: может ли диета помочь в борьбе с раком?
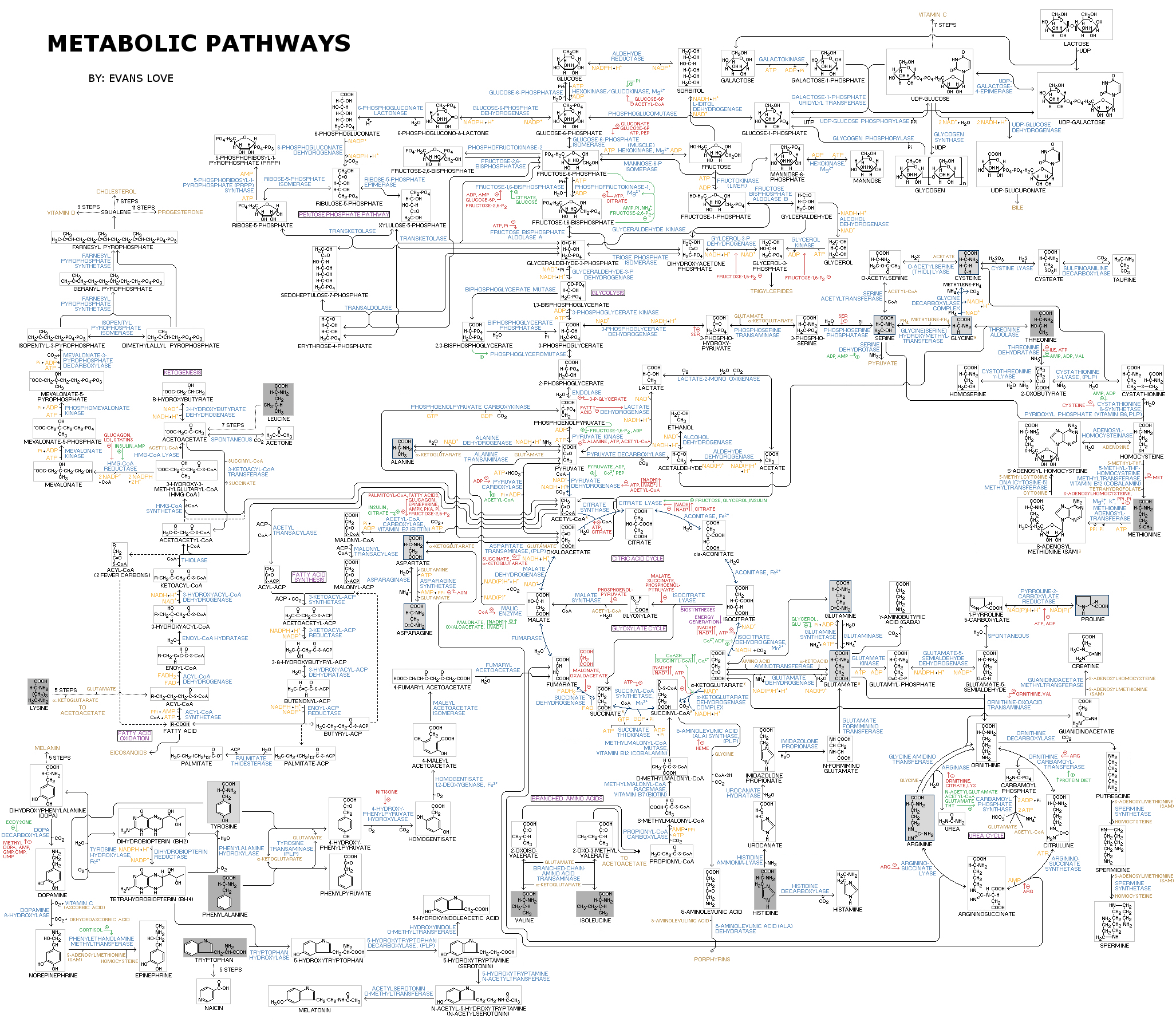
Для того, чтобы разобраться в тонкостях метаболизма раковой клетки, кратко вспомним основные принципы и термины биоэнергетики. Метаболизм — это совокупность химических превращений в клетке, которые направлены на получение энергии и необходимых веществ. Только посмотрите, какое бесчисленное количество реакций включает в себя метаболизм (рис. 3)! Все метаболические пути можно условно разделить на биодеградацию (катаболизм) и биосинтез (анаболизм) [5]. Катаболизм приводит к получению энергии в виде макроэргических соединений (таких как АТФ), а также NADH, NADPH и FADH2 — коферментов, участвующих в окислительно-восстановительных реакциях. Анаболические процессы используют запасенную энергию для синтеза молекул, необходимых для жизни клетки: жиров, нуклеотидов, белков, углеводов.
Рисунок 3. Метаболическая карта — схема, объединяющая основные метаболические пути в клетке.
Метаболизм тесно связан с питанием: ежедневно мы потребляем питательные вещества, которые, с одной стороны, участвуют в катаболических реакциях и поставляют энергию клеткам, а с другой — необходимы для синтеза собственных молекул. Углеводы, белки и жиры, которые мы потребляем, разрушаются в пищеварительном тракте до мономерных единиц: углеводы до моносахаридов (глюкоза, фруктоза и др.), жиры до жирных кислот и глицерина, белки до аминокислот. Эти молекулы поступают в клетки организма и принимают участие в метаболических процессах.
В раковой клетке зачастую увеличена активность некоторых метаболических ферментов или целых метаболических путей, а значит, и потребность в питательных веществах у клеток опухоли может отличаться от нормальных клеток [6]. Эти особенности могут быть учтены при лечении опухоли: исключение из рациона пациента определенных компонентов пищи приведет к понижению их содержания в плазме крови, а следовательно, и в окружении раковых клеток, что негативно скажется на их размножении. Кроме этого, некоторые элементы питания могут непосредственно влиять на противоопухолевый иммунитет, что также должно быть учтено при составлении диеты.
Глюкоза
Глюкоза является основным источником энергии для живых организмов. В нормальном рационе человека она встречается как в свободном виде, так и в составе олиго- и полисахаридов (например, в сахарозе, лактозе и мальтозе). Одним из важнейших биоэнергетических путей в клетке является гликолиз — последовательность химических реакций, в результате которых из 1 молекулы глюкозы получается 2 молекулы пировиноградной кислоты, 2 молекулы АТФ и 2 молекулы NADH. Затем пировиноградная кислота может быть вовлечена в цикл трикарбоновых кислот (цикл Кребса) — биохимический процесс, протекающий в митохондриях, который поставляет NADH и FADH2 что, в конечном счете, делает возможным синтез АТФ посредством окислительного фосфорилирования. При этом из 1 молекулы глюкозы можно получить приблизительно 36 молекул АТФ, что гораздо более выгодно с точки зрения энергетики, нежели просто гликолиз. Вследствие этого большинство клеток активно использует цикл трикарбоновых кислот и окислительное фосфорилирование для получения энергии.
Тем не менее, известно множество случаев, когда по разным причинам клетки смещают баланс в сторону гликолиза, используя этот путь в качестве основного источника энергии, ингибируя ферменты цикла трикарбоновых кислот или активируя ферменты гликолиза.
Давно известно, что опухолевые клетки активно используют гликолиз, несмотря на его относительно низкую эффективность с точки зрения энергетической выгоды. Это явление было открыто Отто Генрихом Варбургом в 1924 году. Сам Варбург считал, что нарушение клеточного дыхания — главная причина развития опухоли. Однако оказалось, что клеточное дыхание в большинстве опухолевых клеток не нарушено, а просто подавляется из-за активного гликолиза. Сейчас понятно, что активный гликолиз дает преимущество опухолевым клеткам. Во-первых, гликолиз протекает без кислорода, и, по-видимому, во многом является адаптацией к гипоксии, которая развивается по мере удаления опухолевых клеток от кровеносных сосудов. Частично эта проблема также решается тем, что раковые клетки могут способствовать ангиогенезу — прорастанию сосудов в опухоль за счет продукции ангиогенных факторов, например фактора роста эндотелия сосудов (VEGF, Vascular endothelial growth factor). Во-вторых, активный гликолиз сопряжен с образованием большого количества молочной кислоты, что приводит к закислению среды, тем самым способствуя инвазии опухоли за счет разрушения нормальных популяции клеток и деградации внеклеточного матрикса.
В то же время, нельзя не отметить тот факт, что эффект Варбурга наблюдается не только в опухолевых клетках, но и вообще во всех активно пролиферирующих клетках. Глюкоза — один из основных источников углерода в клетке, и ее полное окисление в цикле трикарбоновых кислот идет вразрез с потребностями пролиферирующей клетки. Некоторая часть глюкозы, а точнее, ее метаболитов, должна быть направлена на пути биосинтеза аминокислот, нуклеотидов и жирных кислот. Важную роль в производстве предшественников нуклеотидов и аминокислот, а также NADPH, необходимого для синтеза жирных кислот, играет пентозофосфатный путь — альтернативный путь окисления глюкозы, который также имеет ключевое значение в поддержании роста раковых клеток.
Итак, глюкоза особенно необходима раковым клеткам в связи с их активным размножением; при этом она служит не только источником энергии, но и важным предшественником для синтеза аминокислот, нуклеотидов и жирных кислот. Однако помимо непосредственной роли глюкозы в клеточном метаболизме, важным физиологическим аспектом также является эффект инсулина на опухолевые клетки.
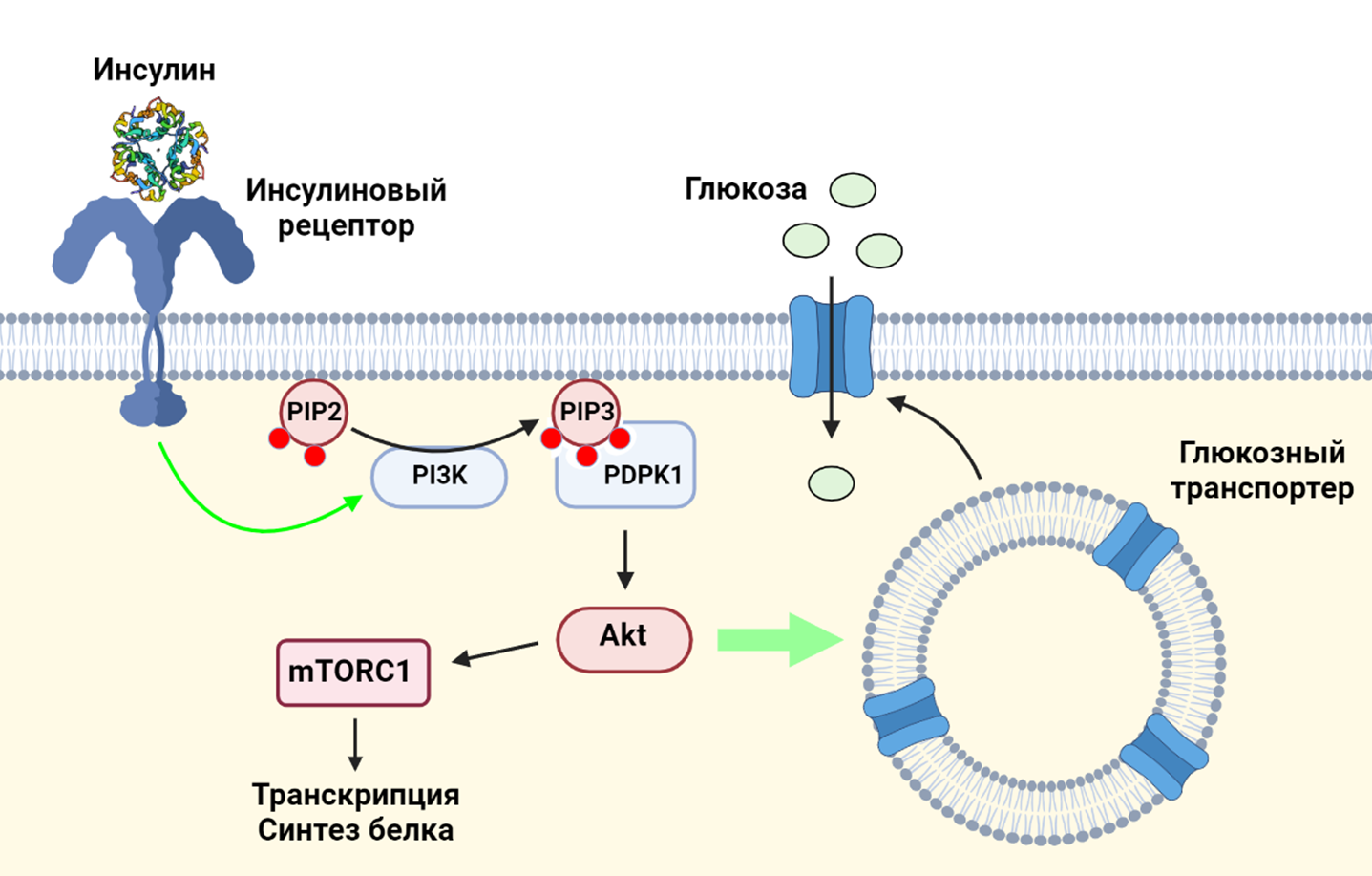
Как известно, повышение уровня глюкозы в крови вызывает секрецию гормона инсулина бета-клетками поджелудочной железы. Инсулин, в свою очередь, взаимодействует с инсулиновыми рецепторами на поверхностях клеток. Взаимодействие инсулина с его рецептором приводит к активации фосфатидилинозитол-3-киназы (PI3K) — ключевого фермента PI3K/AKT/mTOR сигнального пути: работа PI3K делает возможным фосфорилирование протеинкиназы Akt, что приводит, с одной стороны, к транслокации глюкозных транспортеров на клеточную мембрану (и, как следствие, к увеличению поглощения глюкозы клетками), а с другой стороны — к активации протеинкиназы mTORС1, важнейшего регулятора клеточного метаболизма и роста [1].
Рисунок 4. Взаимодействие инсулина и его рецептора приводит к активации фосфатидилинозитол-3-киназы (PI3K), которая фосфорилирует фосфатидилинозитолдифосфат (PIP2). Образовавшийся фосфатидилинозитолтрифосфат (PIP3) нужен для того, чтобы фосфоинозитид-зависимая киназа-1 (PDPK1) активировала протеинкиназу Akt. Akt необходима для стыковки внутриклеточных везикул, несущих глюкозный транспортер, с клеточной мембраной. Также Akt активирует mTORC1.
коллаж авторов статьи. Создан с помощью BioRender.com
Сигнальный путь PI3K/AKT/mTOR играет важную роль в раковых клетках, которые могут активно экспрессировать рецепторы к инсулину и, получая сигналы при их стимуляции, увеличивать темпы роста и размножения.
Снижение уровня глюкозы в крови пациентов рассматривается как одна из потенциальных диетических стратегий при терапии рака. Такой подход ограничит доступность глюкозы для раковых клеток и понизит секрецию инсулина бета-клетками поджелудочной железы. Как можно понизить содержание глюкозы в крови пациентов? Конечно, уменьшение калорийности пищи приведет к снижению уровня глюкозы в крови, но такой способ не может быть оптимальным, так как поставит под угрозу общее состояние пациента. Куда более выгодной стратегией может стать кетогенная диета, которая предполагает ограничение потребления углеводов с одновременным увеличением доли жиров в рационе. Действительно, есть данные доклинических исследований и немногочисленные клинические испытания, которые говорят, что такая диета может способствовать благоприятному исходу болезни — например, при глиобластоме [7]. Однако важно отметить, что некоторые типы опухолей, наоборот, зависят от жирных кислот, а значит, диета, богатая жирами, может опосредовать проканцерогенный эффект [1], о чем мы поговорим чуть далее.
А что насчет других углеводов?
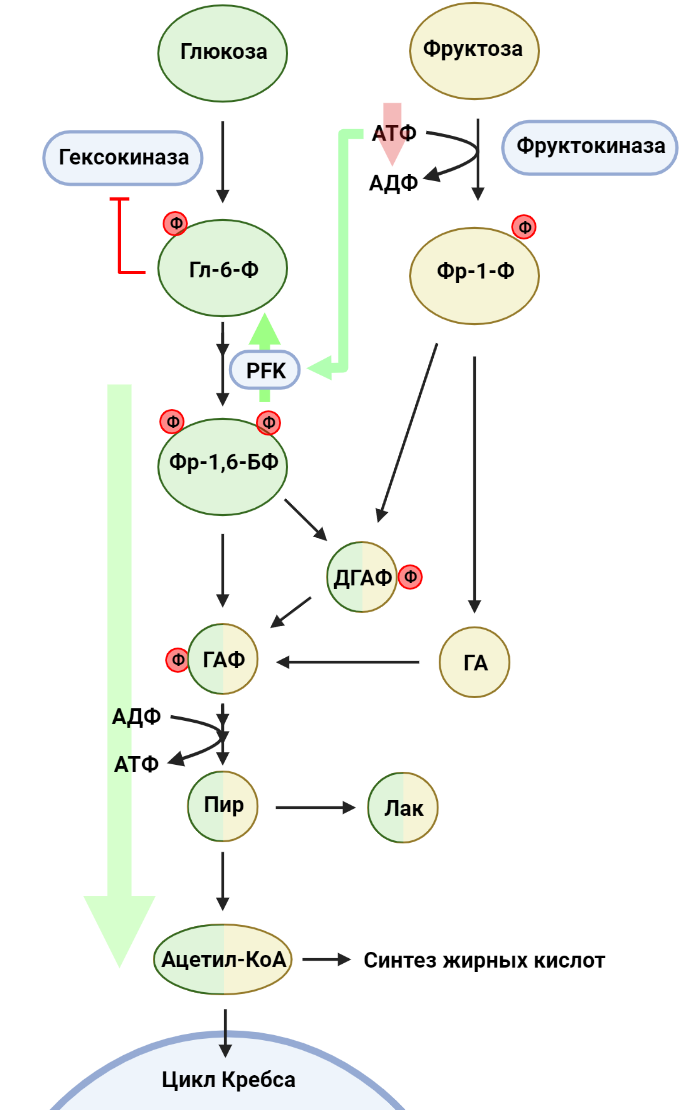
Рисунок 5. Метаболизм фруктозы. В первой стадии гликолиза глюкоза фосфорилируется до глюкозо-6-фосфата (Гл-6-Ф). Параллельно фруктоза фосфорилируется до фруктозо-1-фосфата (Фр-1-Ф). Фруктоза-1,6-бисфосфат (Фр-1,6-БФ), продукт фосфофруктокиназы (PFK), распадается на глицеральдегидфосфат (ГАФ) и дигидроксиацетонфосфат (ДГАФ), а Фр-1,6-БФ расщепляется на ДГАФ и глицеральдегид (ГА). ДГАФ и ГА переходят в ГАФ, который в оставшихся реакциях гликолиза превращается в пируват (ПИР). ПИР может восстановиться до лактата (ЛАК) или подвергаться превращению в ацетил-КоА, соединение, использующееся в многих биохимических процессах.
коллаж авторов статьи. Создан с помощью BioRender.com
Помимо глюкозы, в наш ежедневный рацион входит множество других углеводов. Например, фруктоза, один из наиболее распространенных в природе сахаров, встречается в пище как в свободном виде, так и в составе олигосахаридов, например, сахарозы. Эпидемиологи связывают рост потребления сахаросодержащих напитков с увеличением частоты заболеваемости раком [8]. Более того, оказывается, что даже умеренное потребление фруктозы (эквивалентное одной банке газировки в день) оказывает негативное воздействие и может способствовать росту опухоли, что было отмечено в экспериментах с мышами на примере колоректального рака [9]. Глюкоза эффективно поглощается эпителиальными клетками тонкого кишечника за счет специальных белков, осуществляющих совместный транспорт глюкозы и ионов натрия. При этом транспорт фруктозы опосредуется пассивным транспортером GLUT5 и потому менее эффективен. В результате значительная часть потребляемой фруктозы проходит тонкую кишку и попадает в толстый кишечник. В случае колоректального рака фруктоза становится одним из потенциальных питательных веществ для опухолевых клеток: действительно, раковые клетки в кишечнике активно экспрессируют как GLUT5, так и ферменты, метаболизирующие фруктозу. Глюкоза и фруктоза похожи между собой с точки зрения строения молекул, однако с точки зрения их метаболизма они немного отличаются (рис. 5). Если говорить про глюкозу, то первая стадия гликолиза представляет собой фосфорилирование глюкозы с затратой АТФ и образованием глюкозо-6-фосфата, причем активность гексокиназ (ферментов, осуществляющих эту реакцию) зависит от концентрации глюкозо-6-фосфата в среде: чем больше продукта для фермента, тем менее активно он работает. Это явление — пример отрицательной обратной связи, важного аспекта регуляции активности метаболических путей. Фруктоза же в первую очередь фосфорилируется фруктокиназой до фруктозо-1-фосфата (Фр-1-Ф), также с затратой АТФ, однако в данном случае активность фермента не зависит от концентрации продукта. Это значит, что киназа будет фосфорилировать всю доступную фруктозу, вне зависимости от того, сколько Фр-1-Ф уже было сделано. Следовательно, при повышенной концентрации фруктозы клетка будет тратить много АТФ на ее фосфорилирование. В ответ на понижение уровня АТФ активируется фермент глизолиза фосфофруктокиназа (PFK), а также, помимо этого, продукты расщепления Фр-1-Ф в конечном счете попадают в реакции гликолиза. Таким образом, фруктоза усиливает гликолиз, что на руку раковым клеткам: в случае колоректального рака активация гликолиза способствует индукции синтеза жирных кислот, необходимых для роста опухоли [9].
Надо отметить, что фруктоза, хоть и способствует росту опухолей в случае колоректального рака, для роста и выживания нормальных клеток вовсе не обязательна, так что фармакологическое подавление переносчиков фруктозы и ферментов, участвующих в ее метаболизме (например, фруктокиназы) может препятствовать прогрессии колоректального рака. И конечно же, исключение фруктозы из рациона пациента также может оказывать благотворный эффект на течение болезни. Однако клинических данных, подтверждающих это, пока недостаточно [1].
Еще один любопытный пример связан с маннозой, моносахаридом, который также часто встречается в рационе как в свободном виде, так и в составе полисахаридов. Манноза поглощается теми же транспортерами, что и глюкоза, но затем накапливается в клетках в виде маннозо-6-фосфата и дальше почти не метаболизируется. В то же время, маннозо-6-фосфат ингибирует некоторые ферменты гликолиза (гексокиназу и глюкозоизомеразу), а также глюкозо-6-фосфатдегидрогеназу — первый фермент пентозофосфатного пути, альтернативного способа окисления глюкозы. Таким образом, накопление маннозо-6-фосфат влечет за собой подавление метаболизма глюкозы, что негативно сказывается на жизнеспособности раковых клеток. Однако не все опухоли чувствительны к маннозе. Дело в том, что в клетках есть фермент маннозо-6-фосфат—изомераза (PMI), который катализирует превращение маннозо-6-фосфата в фруктозо-6-фосфат, метаболит гликолиза. Казалось бы, накопление маннозо-6-фосфата перестает быть проблемой для клетки, но дело в том, что разные опухоли имеют разную активность PMI, и если в каких-то опухолевых клетках его активность понижена, то манноза будет подавлять рост опухоли. Оказалось, что колоректальные опухоли обычно имеют очень низкие уровни PMI, и действительно, на мышиной модели колоректального рака было показано, что биодобавки, содержащие маннозу, значительно подавляют рост опухолей и не оказывают отрицательный эффект на здоровье и вес мышей [10]. Возможно, применение маннозы в виде добавок к пище будет повышать эффективность терапии колоректального рака и у людей, но клинических исследований на этот счет еще не проводилось [1].
Жирные кислоты
Жирные кислоты являются важнейшим источником энергии в клетке, особенно для «энергозатратных» тканей вроде скелетной и сердечной мышечных тканей. При окислении жирных кислот (которое в основном происходит в ходе процесса β-окисления) образуются NADH и FADH2, а также ацетил-КоА — вещества, необходимые для синтеза АТФ при окислительном фосфорилировании. Более того, если сравнить между собой жирные кислоты и углеводы, то окажется, что по отношению к своей сухой массе жирные кислоты обеспечивают больше АТФ, чем углеводы, а значит, они лучше подходят на роль запасного питательного вещества (жирные кислоты запасаются в форме триглицеридов в жировой ткани). Разумеется, не могло бы случиться такого, чтобы не нашлось опухолевых клеток, активно использующих жирные кислоты как источник энергии и восстановительных эквивалентов. Действительно, описаны процессы, когда раковая клетка переходит на β-окисление, а также отдельные опухоли, для которых основной источник энергии — это жиры, а не углеводы [1], [11].
Так, было показано, что окисление жирных кислот критично для клеток рака груди при их откреплении от матрикса. Протоки молочных желез выстланы слоем эпителиальных клеток, которые дают начало опухоли. На ранних стадиях развития рака молочной железы опухолевые клетки открепляются от матрикса, покидают свои ниши, начинают пролиферировать в просветах полых железистых структур, заполняя их. Эпителиальные клетки имеют на своей поверхности рецепторы эпидермального фактора роста (epidermal growth factor receptor, EGFR). При стимуляции EGFR, помимо прочего, происходит активация сигнального пути PI3K/AKT/mTOR, что приводит к росту, пролиферации, а также способствует поглощению глюкозы и подавлению апоптоза. Для эпителиальной клетки очень важен контакт с внеклеточным матриксом. Если клетка по какой-либо причине теряет контакт с матриксом, то экспрессия EGFR падает, и, как одно из следствий, клетка начинает испытывать дефицит в глюкозе. В норме эта череда событий непременно приведет к нехватке АТФ, окислительному стрессу, и наконец — к аноикису— гибели клетки, происходящей в ответ на открепление от матрикса. Но опухолевая клетка не так проста и активно пытается спастись от апоптоза. Активность ряда онкогенов в данном случае способствует активации окисления жирных кислот, что обеспечивает клетку энергией и предотвращает гибель [12].
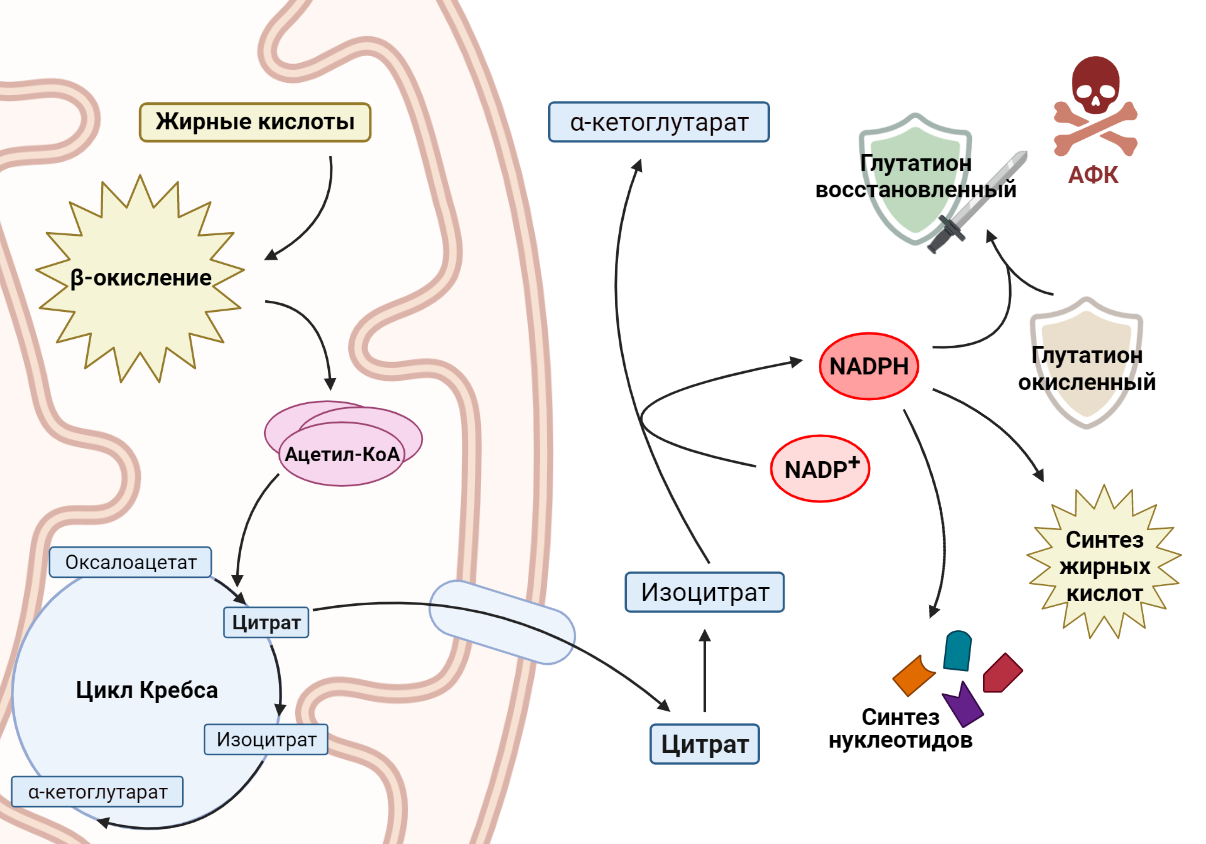
Другой важный пример роли жирных кислот в раковых клетках связан с никотинамидадениндинуклеотидфосфатом (NADPH) — веществом, которое выполняет две основные функции. С одной стороны, он участвует в защите клетки от токсичных активных форм кислорода (АФК), обеспечивая регенерацию антиоксиданта глутатиона (GSH), что особенно важно для выживания раковых клеток в условиях метаболического стресса. С другой стороны, NADPH необходим для синтеза жирных кислот и нуклеотидов, необходимых для поддержания роста и пролиферации клеток, что является неотъемлемой частью биологии опухолевой клетки. Зачастую рост раковой клетки ограничен уровнями NADPH, следовательно, изменения в метаболизме раковой клетки должны учитывать этот важный аспект. Как связаны между собой окисление жирных кислот и производство NADPH? Основным продуктом окисления жиров является ацетил-КоА, который вступает в цикл Кребса и превращается в цитрат. Цитрат может остаться воволеченным в цикл Кребса, а может покинуть митохондрию и выйти в цитоплазму. Там он превратится в изоцитрат, который является субстратом для NADP-зависимой изоцитратдегидрогеназы [13]. Этот фермент окисляет изоцитрат, при этом происходит перенос водорода на NADP+ и образуется NADPH, необходимый раковым клеткам. Например, в клетках глиомы, в которых ингибируется окисление жирных кислот, значительно понижается уровень NADPH, что приводит к накоплению АФК и, как следствие, клеточной гибели [14].
Рисунок 6. Ацетил-КоА, продукт окисления жирных кислот, поступает в цикл Кребса. В то же время цитрат, промежуточное соединение цикла Кребса, покидает митохондрию, где превращается в изоцитрат. При окислении изоцитрата происходит перенос водорода на NADP+, образуется NADPH, необходимый клеткам для множества процессов.
коллаж авторов статьи. Создан с помощью BioRender.com
Из данных примеров мы видим, что в некоторых случаях жирные кислоты способствуют выживанию и метастазированию опухолевых клеток. Это значит, что для отдельных пациентов диета с низким содержанием жиров может оказаться полезной. В то же время, кетогенная диета, которую мы обсуждали в главе про глюкозу, может вызывать непредвиденные проканцерогенные эффекты и способствовать росту опухоли. Таким образом, режим питания пациентов должен подбираться индивидуально с учетом стадии опухоли, ее локализации и особенностей метаболизма.
Аминокислоты
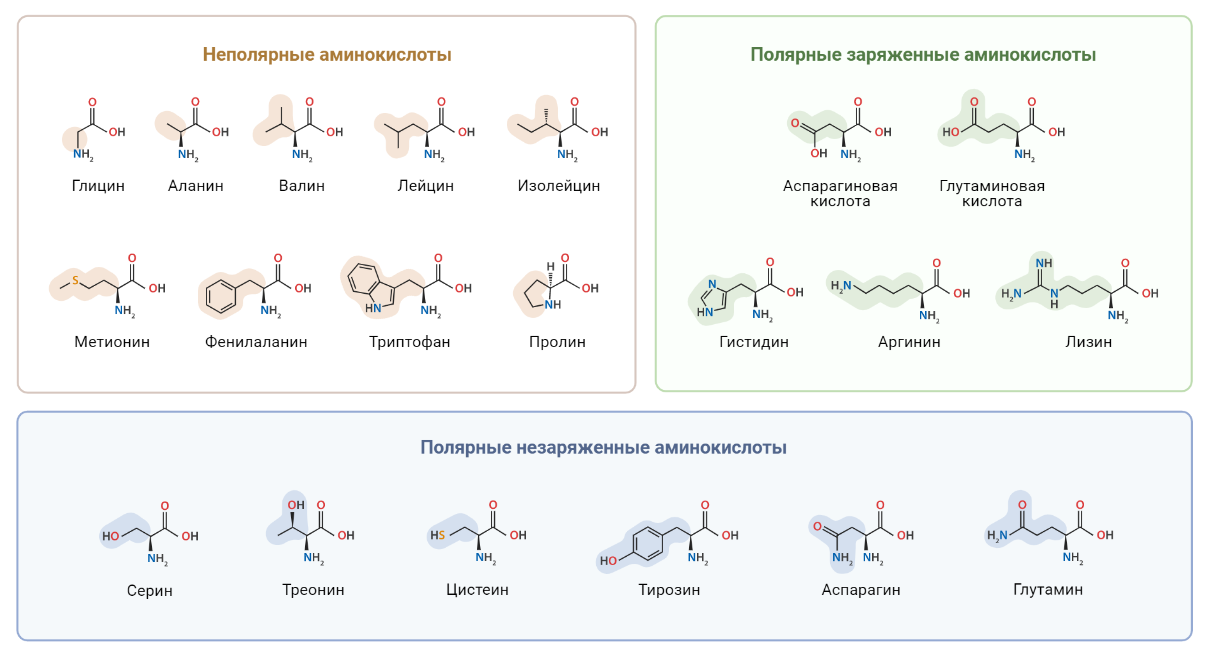
Как известно, белки принимают участие в большинстве клеточных процессов: поддерживают форму клетки, обеспечивают ее подвижность, контролируют работу генов, регулируют метаболические процессы и многое-многое другое. Аминокислоты являются строительными мономерными блоками для белков. Удивительно, что при огромном разнообразии белков, все они построены из довольно ограниченного набора аминокислот (рис. 7).
Рисунок 7. 20 классических аминокислот.
С пищей в организм попадают белки, после чего в желудочно-кишечном тракте они деградируют до отдельных аминокислот. Смесь аминокислот всасывается в тонком кишечнике, поступает в кровь и разносится к каждой клетке организма. В клетках аминокислоты используются уже для синтеза собственных белков, которые необходимы для нормального функционирования организма. Важно отметить, что некоторые из аминокислот клетки нашего организма умеют синтезировать сами (так называемые заменимые аминокислоты), а некоторые непременно должны поступать с пищей (незаменимые аминокислоты). Итак, аминокислоты, которые попали в клетку, могут войти в состав белков, но для нас более интересен тот факт, что отдельные аминокислоты могут выполнять специальные метаболические функции. Далее мы будем рассматривать роль конкретных аминокислот в метаболизме раковых клеток, а также возможные диетические стратегии для пациентов с онкологическими заболеваниями, основанные на ограничении или биодобавках данных аминокислот в рационе.
Метионин
Метионин относится к незаменимым аминокислотам для клеток человека. При этом раковые клетки для своего роста требуют бóльшие количества метионина по сравнению с нормальными клетками. Дело в том, что метионин выполняет ряд регуляторных функций. В клетке есть специальные сенсоры, которые в ответ на высокий уровень метионина (а точнее, его производного — S-аденозилметионина) способны активировать протеинкиназу mTORC1. Эта протеинкиназа крайне важна для раковых клеток: она активирует процесс синтеза белка и, как следствие, ускоряет рост и деление клетки [15]. Кроме этого, S-аденозилметионин является главным донором метильной группы в клетке, то есть обеспечивает метилирование. Метилирование ДНК и гистонов (белков, связанных с ДНК) позволяет «включать» и «выключать» определенные гены. Изменения статуса метилирования гистонов и ДНК регулируют экспрессию генов и вносят свой вклад в рост и развитие опухоли [16]. Начиная с 1990 года проводятся исследования на животных, которые демонстрируют, что ограничение потребления метионина улучшает исход лечения опухолей [1], [17]. Совсем недавно было проведено первое клиническое исследование, которое показало, что снижение количества метионина в рационе пациентов позволяет замедлить прогрессирование опухоли [18]. Таким образом, диетическое ограничение метионина у людей, страдающих онкологическими заболеваниями, является весьма многообещающим подходом [1]. Важно уточнить, что диетическое ограничение тех или иных аминокислот можно осуществить только за счет «искусственных» диет, при которых основным источником белковой пищи являются протеиновые напитки/батончики без содержания определенных аминокислот. Именно такой режим питания соблюдали пациенты, принявшие участие в клиническом испытании диеты с низким содержанием метионина: 75% белковой пищи представляли из себя протеиновые напитки без метионина [18].
Серин
Аминокислота серин принимает участие во множестве метаболических процессов: в синтезе нуклеотидов и липидов; она может превращаться в пируват и поступать в цикл Кребса, и так далее. Серин относится к заменимым аминокислотам и может синтезироваться в нормальных клетках из глюкозы и глицина (самой простой аминокислоты). Для раковых клеток, которые активно используют гликолиз и, соответственно, остро нуждаются в глюкозе, синтез серина из глюкозы непременно обернется потерями в количестве АТФ и скорости размножения. Именно поэтому можно сказать, что для опухолевых клеток серин является незаменимой аминокислотой, то есть обязательно должен поступать извне. Путь синтеза серина из глицина для раковых клеток тоже крайне нежелателен, так как глицин принимает непосредственное участие в синтезе нуклеотидов, а значит, превращение глицина в серин опять же ставит под угрозу скорость деления раковых клеток. Таким образом, ограничение потребление серина действительно может помочь в терапии опухолей. Эффективность такой диеты уже была показана в экспериментах на мышах, но клинических исследований пока не проводилось [1].
Аргинин
В нормальных клетках аргинин способен образовываться de novo, то есть является заменимой аминокислотой. В опухолевых клетках меланомы, гепатоцеллюлярной карциномы и рака простаты синтез аргинина сильно снижен. Это связано с низким уровнем фермента аргининосукцинатсинтетазы, участвующем в образовании аргиинина. Выходит, что некоторые раковые опухоли требуют поступление аргинина извне (для клеток этих опухолей аргинин — незаменимая аминокислота). «Аргининовая зависимость» опухолей может быть использована для терапии, причем как в фармакологических подходах, так и в простом диетическом ограничении аргинина. Про фармакологическое снижение аргинина в раковых клетках уже кое-что известно из научных работ: так, например, препараты, снижающие уровень аргинина в плазме крови пациентов, оказались эффективными при лечении гепатоцеллюлярной карциномы и меланомы [19].
Однако аргинин может негативно сказываться на противоопухолевом иммунитете. Важнейшими клетками, участвующими в борьбе с опухолью, являются T-лимфоциты. Аргинин активно поглощается активированными T-клетками, затем метаболизируется, что приводит к увеличению выживаемости клеток и усилению противоопухолевого Т-клеточного ответа. В мышиной модели рака кожи увеличение количества потребляемого с пищей аргинина привело к уменьшению размера опухолей, способствовало выживанию мышей [20].
Не менее важную роль в противоопухолевом иммунитете играют NK-клетки (Natural killer cells, натуральные киллеры) — иммунные клетки, способные уничтожать опухолевые клетки. Исследования показали, что потребление аргинина с пищей увеличивает количество и активность NK-клеток [21], и, наоборот, дефицит аргинина угнетает работу и жизнеспособность натуральных киллеров [22], что может негативно сказаться на борьбе с опухолью.
Таким образом, аргинин необходим как некоторым опухолям для роста, так и иммунным клеткам, сражающимся с опухолью. По-видимому, только масштабные клинические испытания помогут понять, в каких случаях стоит исключать или, наоборот, увеличивать содержание аргинина в пище для достижения максимального эффекта терапии.
Цистин и цистеин
Одна из важнейших функций аминокислоты цистеина в клетке — защита от активных форм кислорода (например, перекиси водорода), которые повреждают ДНК, липиды и белки, вызывая в клетке окислительный стресс. Раковые клетки, по сравнению с нормальными, испытывают сильный окислительный стресс и требуют большого количества цистеина. Действительно, для некоторых опухолевых клеток снижение уровня цистеина губительно: клетки «сгорают» из-за накопленных активных форм кислорода. Цистеин образуется из неклассической аминокислоты цистина, которая поступает в клетку из плазмы крови [1]. Препараты, снижающие уровень цистина в плазме крови, тормозят рост опухолей с мутантным рецептором эпидермального фактора роста (например, немелкоклеточного рака легких) у мышей [23]. Теоретически, достичь снижения уровня цистина в плазме крови пациентов можно при помощи корректировки диеты, без применения препаратов, но такой подход пока не исследован.
Гистидин
При деградации гистидина в клетке тратится тетрагидрофолат — кофактор, который необходим для синтеза нуклеотидов, а значит, определяет скорость деления раковых клеток. Чем больше в раковую клетку поступает гистидина, тем больше тетрагидрофолата тратится на распад гистидина и тем медленнее клетка делится. Применение гистидина вместе с пищей может помочь в терапии некоторых видов опухолей. В частности, такой диетический подход может стать особенно эффективным при лечении рака химиотерапевтическим агентом — метотрексатом (часто применяется для лечения злокачественных заболеваний крови). Метотрексат нарушает синтез тетрагидрофолата, что приводит к остановке синтеза нуклеотидов и к гибели раковых клеток. Оказалось, что эффективность лечения лейкемии метотрексатом заметно увеличивается при добавлении к пище аминокислоты гистидина — это было показано на мышиной модели [24].
Биодобавки фолиевой кислоты
В заключение мы хотим уделить внимание витаминам. Витамины необходимы для протекания многих биохимических реакций и должны поступать в организм с пищей. Существует распространенное заблуждение о том, что прием витаминных биодобавок может послужить защитой от рака и других заболеваний. На самом деле, витамины должны поступать исключительно с пищей, а дополнительный прием витаминов здоровым людям в основном не рекомендован (за некоторыми редкими исключениями). Регулярный прием биодобавок может оказаться не только неэффективными, но и вредным, особенно людям, страдающим онкологическими заболеваниями. Давайте рассмотрим пример того, как дополнительный прием витаминов способствует росту опухоли.
Фолиевая кислота (фолат, витамин B9) является необходимым веществом для синтеза нуклеотидов. Опухолевые клетки быстро делятся и нуждаются в больших количествах нуклеотидов для синтеза ДНК, поэтому активно потребляют фолат. Еще в 1948 году стало известно, что биодобавки фолиевой кислоты способствуют росту некоторых видов опухолей [25]. На сегодняшний день метаболизм фолиевой кислоты является фармакологической мишенью для терапии рака: упоминавшийся ранее химиотерапевтический препарат метотрексат нарушает метаболизм фолата и ингибирует пути синтеза нуклеотидов. Надо подчеркнуть, что антифолиевая терапия рака пока что является сугубо фармакологической и не предполагает корректировки диеты [1].
Однако потенциальные негативные эффекты фолата в опухолевой прогрессии на этом не заканчиваются. Ряд исследований показал, что присутствие в крови неметаболизированной фолиевой кислоты, связанное с ее избыточным потреблением, влекло за собой снижение количества и активности NK-клеток [26-28]. Упоминавшиеся ранее NK-клетки — это иммунные клетки, одна из основных функций которых состоит в защите организма от раковых клеток. Следовательно, снижение числа и подавление активности NK-клеток может повлечь за собой повышенный риск образования и прогрессии рака, хотя конкретных исследований о влиянии высоких доз фолата на противоопухолевый иммунитет не проводилось.
Таким образом, витамины необходимы для поддержания функций организма, однако чрезмерное потребление некоторых из них может привести к негативным последствиям, в том числе и к прогрессии опухоли, как в случае с витамином B9. Возможно, диета с низким содержанием фолата будет полезной для некоторых пациентов.
Заключение
Мы постарались кратко охарактеризовать некоторые особенности метаболизма опухолевых клеток и роль питательных веществ в прогрессии рака. В заключение мы хотели бы еще раз обратить внимание на то, что не существует какой-либо универсальной диеты для людей, страдающих онкологическими заболеваниями. Это связано с тем, что опухоли сильно различаются по своему метаболизму. Перечисленные диетические подходы пока что не могут использоваться повсеместно, так как перед внедрением любого из них для каждого типа рака, его локализации и стадии заболевания должны быть проведены масштабные клинические испытания, подтверждающие безопасность и эффективность нового метода лечения. Однако, ввиду многообещающих результатов исследований, модификации диеты являются перспективным подходом к лечению рака. Мы уверены, что в скором времени контроль состава диеты пациентов станет важной частью терапии онкологических заболеваний и поможет спасти многие жизни. А пока что давайте просто стараться питаться правильно и вести здоровый образ жизни. Будьте здоровы!
- Naama Kanarek, Boryana Petrova, David M. Sabatini. (2020). Dietary modifications for enhanced cancer therapy. Nature. 579, 507-517;
- Путь клетки «из греков в варяги». Малигнизация: причины и следствия;
- Douglas Hanahan, Robert A Weinberg. (2000). The Hallmarks of Cancer. Cell. 100, 57-70;
- Douglas Hanahan, Robert A. Weinberg. (2011). Hallmarks of Cancer: The Next Generation. Cell. 144, 646-674;
- Метаболизм клетки;
- Вослед Варбургу — последние достижения в изучении биоэнергетики рака;
- Colin E. Champ, Joshua D. Palmer, Jeff S. Volek, Maria Werner-Wasik, David W. Andrews, et. al.. (2014). Targeting metabolism with a ketogenic diet during the treatment of glioblastoma multiforme. J Neurooncol. 117, 125-131;
- Julie K. Bassett, Roger L. Milne, Dallas R. English, Graham G. Giles, Allison M. Hodge. (2020). Consumption of sugar‐sweetened and artificially sweetened soft drinks and risk of cancers not related to obesity. Int. J. Cancer. 146, 3329-3334;
- Marcus D. Goncalves, Changyuan Lu, Jordan Tutnauer, Travis E. Hartman, Seo-Kyoung Hwang, et. al.. (2019). High-fructose corn syrup enhances intestinal tumor growth in mice. Science. 363, 1345-1349;
- Pablo Sierra Gonzalez, James O’Prey, Simone Cardaci, Valentin J. A. Barthet, Jun-ichi Sakamaki, et. al.. (2018). Mannose impairs tumour growth and enhances chemotherapy. Nature. 563, 719-723;
- Arkaitz Carracedo, Lewis C. Cantley, Pier Paolo Pandolfi. (2013). Cancer metabolism: fatty acid oxidation in the limelight. Nat Rev Cancer. 13, 227-232;
- Zachary T. Schafer, Alexandra R. Grassian, Loling Song, Zhenyang Jiang, Zachary Gerhart-Hines, et. al.. (2009). Antioxidant and oncogene rescue of metabolic defects caused by loss of matrix attachment. Nature. 461, 109-113;
- Alessandra Castegna, Pasquale Scarcia, Gennaro Agrimi, Luigi Palmieri, Hanspeter Rottensteiner, et. al.. (2010). Identification and Functional Characterization of a Novel Mitochondrial Carrier for Citrate and Oxoglutarate in Saccharomyces cerevisiae. Journal of Biological Chemistry. 285, 17359-17370;
- Lisa S. Pike, Amy L. Smift, Nicole J. Croteau, David A. Ferrick, Min Wu. (2011). Inhibition of fatty acid oxidation by etomoxir impairs NADPH production and increases reactive oxygen species resulting in ATP depletion and cell death in human glioblastoma cells. Biochimica et Biophysica Acta (BBA) — Bioenergetics. 1807, 726-734;
- Xin Gu, Jose M. Orozco, Robert A. Saxton, Kendall J. Condon, Grace Y. Liu, et. al.. (2017). SAMTOR is an
S
-adenosylmethionine sensor for the mTORC1 pathway. Science. 358, 813-818; - Samantha J. Mentch, Mahya Mehrmohamadi, Lei Huang, Xiaojing Liu, Diwakar Gupta, et. al.. (2015). Histone Methylation Dynamics and Gene Regulation Occur through the Sensing of One-Carbon Metabolism. Cell Metabolism. 22, 861-873;
- Raghu Sinha, Timothy K. Cooper, Connie J. Rogers, Indu Sinha, William J. Turbitt, et. al.. (2014). Dietary methionine restriction inhibits prostatic intraepithelial neoplasia in TRAMP mice. Prostate. 74, 1663-1673;
- Xia Gao, Sydney M. Sanderson, Ziwei Dai, Michael A. Reid, Daniel E. Cooper, et. al.. (2019). Dietary methionine influences therapy in mouse cancer models and alters human metabolism. Nature. 572, 397-401;
- Francesco Izzo, Paolo Marra, Gerardo Beneduce, Giuseppe Castello, Paolo Vallone, et. al.. (2004). Pegylated Arginine Deiminase Treatment of Patients With Unresectable Hepatocellular Carcinoma: Results From Phase I/II Studies. JCO. 22, 1815-1822;
- Roger Geiger, Jan C. Rieckmann, Tobias Wolf, Camilla Basso, Yuehan Feng, et. al.. (2016). L-Arginine Modulates T Cell Metabolism and Enhances Survival and Anti-tumor Activity. Cell. 167, 829-842.e13;
- K.G.M. Park, P.D. Hayes, O. Eremin, H. Sewell, K.G.M. Park, P.J. Garlick. (1991). Stimulation of lymphocyte natural cytotoxicity by L-arginine. The Lancet. 337, 645-646;
- Bruno Lamas, Juliette Vergnaud-Gauduchon, Nicolas Goncalves-Mendes, Olivier Perche, Adrien Rossary, et. al.. (2012). Altered functions of natural killer cells in response to L-Arginine availability. Cellular Immunology. 280, 182-190;
- Ioannis Poursaitidis, Xiaomeng Wang, Thomas Crighton, Christiaan Labuschagne, David Mason, et. al.. (2017). Oncogene-Selective Sensitivity to Synchronous Cell Death following Modulation of the Amino Acid Nutrient Cystine. Cell Reports. 18, 2547-2556;
- Naama Kanarek, Heather R. Keys, Jason R. Cantor, Caroline A. Lewis, Sze Ham Chan, et. al.. (2018). Histidine catabolism is a major determinant of methotrexate sensitivity. Nature. 559, 632-636;
- Sidney Farber, Louis K. Diamond, Robert D. Mercer, Robert F. Sylvester, James A. Wolff. (1948). Temporary Remissions in Acute Leukemia in Children Produced by Folic Acid Antagonist, 4-Aminopteroyl-Glutamic Acid (Aminopterin). N Engl J Med. 238, 787-793;
- Hathairat Sawaengsri, Junpeng Wang, Christina Reginaldo, Josiane Steluti, Dayong Wu, et. al.. (2016). High folic acid intake reduces natural killer cell cytotoxicity in aged mice. The Journal of Nutritional Biochemistry. 30, 102-107;
- Aron M. Troen, Breeana Mitchell, Bess Sorensen, Mark H. Wener, Abbey Johnston, et. al.. (2006). Unmetabolized Folic Acid in Plasma Is Associated with Reduced Natural Killer Cell Cytotoxicity among Postmenopausal Women. The Journal of Nutrition. 136, 189-194;
- Clovis Paniz, Juliano Felix Bertinato, Maylla Rodrigues Lucena, Eduardo De Carli, Patrícia Mendonça da Silva Amorim, et. al.. (2017). A Daily Dose of 5 mg Folic Acid for 90 Days Is Associated with Increased Serum Unmetabolized Folic Acid and Reduced Natural Killer Cell Cytotoxicity in Healthy Brazilian Adults. The Journal of Nutrition. 147, 1677-1685.
БАД к пище.
Действие конкретного продукта определяется биологическими свойствами активных веществ, входящих в его состав.
В состав используемой биологически активной добавки к пище могут быть включены не все перечисленные ниже активные вещества.
Полифенольные соединения — это природные органические вещества, в молекуле которых имеется 2 или более фенольные группы. Являются антиоксидантами. Способны оказывать бактерицидное действие, улучшают состояние иммунной системы, уменьшают проницаемость капилляров. К полифенольным соединениям относятся флавоноиды, танин; лигнаны.
Флавоноиды широко распространены в растительном мире. Они обладают выраженными антиоксидантными свойствами, различным флавоноидам присущи антиаллергенные, противовоспалительные, антивирусные, антибактериальные свойства и другие типы биологической активности. В растениях флавоноиды встречаются в виде флавоногликозидов и в свободном виде.
К основным классам флавоноидов относятся флаваноны (гесперидин, нарингин), дигидрохалконы, халконы, флаваны (катехин, антоцианидины), флаванонолы (дигидрофлавонолы), флавонолы (кверцетин, дигидрокверцетин, рутин), флавоны (апигенин, лютеолин), и изофлавоноиды.
Катехины – соединения растительного происхождения. Широко распространены в природе катехин и его диастереомер – эпикатехин. Обладают высокой биологической активностью: регулируют проницаемость капилляров. Катехины содержатся во многих растениях и продуктах растительного происхождения, являются сильными антиоксидантами. Обладают целым рядом полезных свойств, в т.ч. способствуют укреплению стенки капилляров, более эффективному использованию организмом аскорбиновой кислоты; задерживают развитие дегенеративных заболеваний костной ткани; способствуют улучшению состояния кожи; проявляют антибактериальные и противовоспалительные свойства; могут подавлять Helicobacter pylori, не затрагивая при этом полезные микроорганизмы кишечной биоты.
Антиоксидантные свойства катехинов в несколько раз сильнее, чем у витаминов С и Е.
Танины (дубильные кислоты) – органические вещества природного происхождения. Больше всего танинов содержится в коре дуба. Придают терпкий вкус фруктам, винам, содержатся в чае. Отличие дубильных веществ от других полифенольных соединений — это способность образовывать прочные водородные связи с белками.Обладают вяжущими, антибактериальными, кровоостанавливающими и противовоспалительными свойствами.
Антоцианидины – в растениях присутствуют в виде гликозидов (антоцианов). Придают растительным тканям разнообразную окраску – от розовой до черно-фиолетовой.
Гесперидин — биофлавоноид. Уменьшает растяжимость вен, повышает их тонус, что способствует снижению венозного застоя; уменьшает проницаемость капилляров и повышает их резистентность, улучшает микроциркуляцию и лимфоотток.
Лигнаны – в наибольшем количестве содержатся в лимоннике китайском. Лигнаны лимонника — схизандрины, обладают тонизирующей активностью. Элеутерозиды — лигнаны элеутерококка — повышают синтез эндорфинов, вызывающих расщепление жиров и высвобождение их в кровь. Активизируют метаболизм углеводов, предотвращая превращение последних в жиры.
Рутозид (рутин) — ангиопротектор. Относится к группе витамина P. Устраняя повышенную проницаемость капилляров, укрепляет сосудистую стенку, уменьшает ее отечность и воспаление. Обладает антиагрегантным действием, что способствует улучшению микроциркуляции. Замедляет развитие диабетической ретинопатии. При местном применении оказывает также охлаждающее и успокаивающее действие.
Витамин С (аскорбиновая кислота) обеспечивает синтез коллагена; участвует в формировании и поддержании структуры и функции хрящей, костей, зубов; влияет на образование гемоглобина, созревание эритроцитов.
Витамин Е (α-токоферола ацетат) обладает антиоксидантными свойствами, поддерживает стабильность эритроцитов, предупреждает гемолиз; оказывает положительное влияние на функции половых желез, нервной и мышечной ткани.
Каротиноиды (бетакаротен, лютеин, ликопин) являются природными органическими пигментами, синтезируемыми бактериями, грибами, водорослями, высшими растениями и коралловыми полипами; окрашены в желтый, оранжевый или красный цвета. Бетакаротен является предшественником витамина А. Оказывает антиоксидантное действие, обладает способностью инактивировать свободные радикалы в условиях гипоксии. Обладает иммуномодулирующим действием. Повышает устойчивость организма к инфекциям.
Кофеин — повышает умственную и физическую работоспособность, стимулирует психическую деятельность, двигательную активность, укорачивает время реакций, временно уменьшает утомление и сонливость.
Органические кислоты, в т.ч. гидроксилимонная, группа гидроксикоричных кислот содержатся преимущественно в продуктах растительного происхождения: во фруктах, ягодах, некоторых овощах и продуктах их переработки. Считается, что органические кислоты способствую ускорению физиологических процессов.
Панаксозиды – тритерпеновые гликозиды, основным источником является корень женьшеня. Повышают устойчивость организма к вредным физическим, химическим и биологическим факторам. Иммуностимулирующее действие их выражается в стимуляции продукции антител, сопровождающейся увеличением количества общего белка и гамма-глобулинов в крови. Панаксозиды стимулируют кроветворение, почти в 2 раза усиливают биосинтез нуклеиновых кислот, белков и жиров в костном мозге.Способствуют нормализации работы органов и различных функций организма.
Эсцин — тритерпеновый гликозид (сапонин) из плодов (семян) конского каштана. Обладает выраженной капилляропротективной активностью, оказывает антиэкссудативное действие.
Салидрозид — фенольный гликозид, в значительном количестве содержится в корнях и корневище родиолы розовой и родиолы четырехраздельной, в коре ивы; обладает стимулирующим и адаптогенным действием.
Арбутин — фенольный гликозид, в организме человека расщепляется на гидрохинон и глюкозу. Обладает выраженными антисептическими свойствами. Содержится во многих растениях, в т.ч. в грушанке, бруснике, толокнянке, шелковице, бадане, кавказской чернике. Активное соединение оказывает значительное антисептическое действие на мочевыводящие пути.
В России у 3 762 218 человек диагностированы злокачественные новообразования и каждый год эта цифра увеличивается более чем на 600 000 новых случаев [1]. Всем онкопациентам необходимо противоопухолевое лечение, и многим из них – лекарственное.
Большую часть лекарственного противоопухолевого лечения пациенты, как правило, получают с помощью внутривенных инъекций. Это предполагает регулярное посещение онкологического учреждения для проведения очередного цикла терапии. Нередко это приносит неудобства, а инъекции могут быть болезненными. В некоторых случаях количество циклов не ограничено определенным числом, лечение может длиться месяцы или годы, вплоть до прогрессирования или развития непереносимой токсичности [2].
Чтобы пациент мог сократить количество визитов в больницу, все больше новых препаратов производится в пероральной форме.
Что такое пероральная лекарственная противоопухолевая терапия?
- Пероральная терапия – это любая терапия, которая принимается внутрь через рот в виде таблеток или капсул.
Безусловно такое лечение позволяет человеку вести активную жизнь и работать, что особенно актуально при длительной противоопухолевой терапии.
Таблетки – это только химиотерапия?
Не только. Ниже представлены основные препараты, которые можно использовать внутрь перорально:
- Химиотерапия: циклофосфамид, метотрексат, этопозид, капецитабин, винорелбин;
- Гормонотерапия: тамоксифен, торемифен, анастрозол, летрозол, эксеместан, мегестрол, медроксипрогестерон, бикалутамиб, энзалутамид, абиратерон;
- Таргетная терапия: регорафениб, сорафениб, сунитиниб, пазопаниб, акситиниб, гефитиниб, эрлотиниб, афатиниб, осимертиниб, кризотиниб, олапариб, палбоциклиб, рибоциклиб, лапатиниб, дабрафениб, траметиниб, вемурафениб, кобиметиниб.
Почему мне выписали таблетки, а моей знакомой с таким же диагнозом — капельницы?
Если вам назначили таблетки — это не значит, что исчерпаны все возможности вашего лечения.
Таблетки или капсулы могут назначаться как самостоятельное лечение, так и в качестве послеоперационного (после радикального удаления опухоли) профилактического (адъювантного) лечения. Пример таблетированной адъювантной терапии при раке молочной железы – тамоксифен или анастрозол в течение 5 лет [3].
В каких случаях могут назначить «химию» в таблетках?
Таблетки или капсулы назначают по определенным показаниям:
- Гистологический тип опухоли. Например, аденокарцинома.
- Рецепторный статус опухоли. Например, наличие рецепторов к эстрогену и прогестерону [3].
- Другие характеристики опухоли. Например, наличие определенной мутации, степень злокачественности, стадия распространения, наличие лимфоваскулярной инвазии и т.д.
- Важно и состояние вашего желудочно-кишечного тракта, а именно — возможность усвоить и произвести всасывание лекарственного препарата в системный кровоток.
Таблетки также могут применяться в следующих случаях:
- Пораженные вены;
- Невозможность внутривенного введения;
- Отек верхних конечностей;
- Поражение кожи грудной стенки, когда нет возможности установить порт-систему.
Например, пациенту может быть назначена поддерживающая лечебная химиотерапия капецитабином вместо внутривенного 5-фторурацила с лейковорином [4].
При опухолях каких органов могут назначить таблетки?
Рак молочной железы [5]:
- Химиотерапия (метастатический процесс): CMF (циклофосфамид внутрь + метотрексат в/в + 5-фторурацил в/в); Метрономный режим циклофосфамид + метотрексат; Капецитабин; Винорелбин (капсулы); Этопозид (капсулы).
- Гормонотерапия (послеоперационно или при метастатическом процессе): Тамоксифен, Анастрозол, Летрозол, Эксеместан, Мегестрол.
- Таргетная терапия (метастатический процесс): Рибоциклиб, Палбоциклиб, Лапатиниб.
- Остеомодифицирующий агент (при метастазах в костях): Клодроновая кислота.
Рак ободочной и прямой кишки [6,7]:
- Химиотерапия (послеоперационно или при метастатическом процессе): в схеме CapOX (XELOX) – Капецитабин внутрь + Оксалиплатин внутривенно, Капецитабин.
- Таргетная терапия (при метастатическом процессе): Регорафениб.
Рак яичников [8]:
- Химиотерапия (метастатический процесс): этопозид; циклофосфамид + метотрексат (метрономный режим).
- Гормонотерапия (метастатический процесс): летрозол, анастрозол, тамоксифен.
- Таргетная терапия (метастатический процесс или рецидив): Олапариб.
Рак тела матки (метастатический процесс) [9]: гормонотерапия (летрозол, анастрозол, тамоксифен).
Рак шейки матки (метастатический процесс) [10]: капецитабин.
Немелкоклеточный рак легкого (метастатический процесс) [11]: Гефитиниб, Эрлотиниб, Афатиниб, Осимертиниб, Кризотиниб.
Почечно-клеточный рак (метастатический процесс) [12]: Сорафениб, Сунитиниб, Пазопаниб и Акситиниб.
Меланома кожи (послеоперационно или при метастатическом процессе) [13]: Дабрафениб, Траметиниб, Вемурафениб, Кобиметиниб.
Меньше ли осложнений от таблеток или капсул?
Нет, таблетки и капсулы — это все равно противоопухолевая терапия. Она отличается лишь способом доставки лекарственного средства в организм. Осложнения и побочные эффекты такие же, как и при инъекциях.
Потеряю ли я волосы от противоопухолевой лекарственной терапии в таблетках?
Да, в некоторых случая это возможно [14], например:
- Этопозид вызывает обратимую алопецию у 8–66% пациентов, а иногда вызывает полную потерю волос;
- Метотрексат, Винорелбин и Циклофосфамид часто вызывают умеренную алопецию;
- Капецитабин редко вызывает выпадение волос.
Будет ли тошнота и рвота при пероральной противоопухолевой лекарственной терапии?
Да, некоторые препараты больше других вызывают рвоту [15]:
- Для Циклофосфамида, Винорелбина и Кризотиниба характерна умеренная эметогенность, т.е. рвота возникает у 30-90% пациентов. Для профилактики обязательно назначается противорвотная терапия.
- Капецитабин, этопозид и большинство таргетных препаратов относятся к препаратам с низкой эметогенностю, т.е. рвота возникает у 10-30% пациентов
- Метотрексат и Вемурафениб обладают минимальной эметогенностью (рвота у <10%) и не требуют назначения противорвотных средств.
- Еще реже вызывает рвоту гормональная терапия.
Какие еще осложнения возможны при приеме противоопухолевой терапии в таблетках и капсулах?
- Изменения со стороны крови: анемия, лейкопения, нейтропения, тромбоцитопения;
- Изменения кожи (капецитабин – ладонно-подошвенный синдром [16]; регорафениб, сорафениб, сунитиниб и акситиниб – ладонно-подошвенная кожная реакция [17]);
- Стоматит;
- Слабость;
- Диарея;
- Дисменорея, приливы, вагинальное кровотечение (гормональная терапия [18]).
О чем мне стоит знать до начала пероральной противоопухолевой лекарственной терапии?
- В каких дозах и когда принимать (сколько раз в день; после, до или во время еды);
- Сопутствующие мероприятия (пить много жидкости до, во время и после приема циклофосфамида [19]; с какими продуктами совместимо);
- Обязательно сообщить врачу, какие препараты вы принимаете по сопутствующим заболеваниям (артериальная гипертензия, сахарный диабет и т.д.), чтобы предусмотреть возможные взаимодействия;
- Ваш лечащий врач может не помнить все особенности приема всех пероральных средств. Нет ничего зазорного, чтобы уточнить особенности приема вашего препарата. Спрашивать не только можно, но и нужно!
Какие существуют особенности приема внутрь отдельных противоопухолевых препаратов?
- Этопозид: внутрь, натощак (можно принимать, запивая стаканом апельсинового сока). Избегать действий, которые могут привести к травмам и кровотечениям (включая бритье).
- Метотрексат: избегать действий, которые могут привести к травмам и кровотечениям (включая бритье); избегать солнца.
- Винорелбин: внутрь, целиком, не разжевывая и не рассасывая во рту, запивая водой. В связи с наличием сорбита, винорелбин не следует использовать у больных с наследственной непереносимостью фруктозы.
- Тамоксифен: внутрь, не разжевывая, запивая водой. В начале лечения в течение 2 недель возможно увеличение мягкотканных образований и эритема пораженных областей.
- Анастрозол, Летрозол: внутрь целиком, в одно и то же время, запивая водой. Применяется только в постменопаузе или у пациенток с овариальной супрессией.
- Эксеместан: внутрь, желательно после еды. Применяется только в постменопаузе или у пациенток с овариальной супрессией.
- Сунитиниб: внутрь, независимо от приема пищи. Может наблюдаться изменение окраски кожи вследствие наличия в препарате желтого красителя.
- Акситиниб: внутрь целиком, запивая стаканом воды, вне зависимости от приема пищи;
- Сорафениб: внутрь, в промежутках между приемами пищи или вместе с пищей, содержащей низкое или умеренное количество жира, запивая стаканом воды.
- Регорафениб: внутрь целиком, запивая водой, 1 раз в сутки в одно и то же время после приема пищи, содержащей низкое (<30%) количество жиров.
- Пазопаниб: внутрь целиком 1 раз в сутки, не менее чем за 1 час до или через 2 часа после приема пищи.
- Гефитиниб: внутрь, независимо от приема пищи, 1 раз в сутки. Можно также растворить (в течение 15 минут) в 100 мл питьевой (негазированной) воды и вводить внутрь через назогастральный зонд. N.B! В составе препарата – лактоза (необходимо учитывать непереносимость)!
- Эрлотиниб: внутрь, 1 раз в сутки, не менее чем за 1 час или через 2 часа после приема пищи. Курение снижает концентрацию эрлотиниба в плазме крови на 50–60%
- Афатиниб: внутрь, натощак, не менее чем за 1 ч до приема пищи или спустя 3 часа после приема пищи.
- Осимертиниб: внутрь целиком, 1 раз в сутки, в одно и то же время вне зависимости от приема пищи. Можно растворить в 15 мл питьевой (негазированной) воды и вводить через назогастральный зонд
- Кризотиниб: Внутрь целиком, вне зависимости от приема пищи. Избегать употребления грейпфрута и грейпфрутового сока
- Олапариб (табл., капс.): Внутрь целиком, через 1 час после или за 2 часа до приема пищи. B! Дозы таблеток и капсул не взаимозаменяемы!
- Палбоциклиб: внутрь целиком вместе с пищей в одно и то же время. Избегать грейпфрута или грейпфрутового сока, а также препаратов зверобоя.
- Рибоциклиб: внутрь целиком вне зависимости от приема пищи в одно и то же время.
- Лапатиниб: внутрь, за 1 час до или через 1 час после еды. Суточную дозу нельзя делить на приемы.
- Дабрафениб: внутрь 2 раза в сутки в одно и то же время через 1 час после или за 2 часа до приема пищи. Может быть повышение уровня глюкозы, что потребует изменения доз препаратов для лечения сахарного диабета.
- Траметиниб: внутрь 1 раз в сутки в одно и то же время, через 1 час после или за 2 часа до приема пищи.
- Вемурафениб: внутрь целиком 2 раза в сутки, вне зависимости от приема пищи, однако следует воздержаться от длительного приема обеих доз натощак.
- Кобиметиниб: внутрь целиком 1 раз в сутки, вне зависимости от приема пищи.
- Клодроновая кислота: внутрь. Суточная доза 1600 мг однократно утром натощак (за 1 час до еды), запивая стаканом воды (если >1600 мг, то в 2 приема). Нельзя принимать вместе с молоком, пищей и препаратами, содержащими двухвалентные катионы (кальций, препараты железа, антациды). Избегать стоматологических вмешательств во время приема клодроновой кислоты. До начала приема клодроновой кислоты следует санировать полость рта.
Что делать в случае пропуска приема таблетки(-ок)?
- Сообщить об этом вашему лечащему врачу
- В следующий прием НИКОГДА не принимайте дополнительно пропущенную дозу! *
* За исключением некоторых случаев. Необходимо ознакомиться с инструкцией к препарату.
Как не забыть принять противоопухолевые лекарства?
- Принимать таблетки в одно и то же время и при одних и тех же обстоятельствах каждый день.
- Поставьте напоминание на своем смартфоне.
- В путешествие возьмите с собой достаточно таблеток на случай непредвиденных задержек.
- Ведите дневник с информацией о вашем самочувствии. Держите дневник на видном месте.
- Просите родственников напоминать о приеме лекарств.
Что делать, если выпил двойную (и более) дозу?
- Немедленно сообщить об этом лечащему врачу.
- Тщательно следить за состоянием своего здоровья (вести дневник).
- В некоторых случаях потребуются срочные мероприятия (например, введение кальция фолината при передозировке метотрексата в течение первого часа).
Мне дали пачку таблеток – я могу просто пить таблетки и больше ничего не делать?
Нет, при каждом из препаратов требуется периодически выполнять обследования с целью выявления возможных осложнений лечения. Примеры:
- Клинический и биохимический анализы крови (ОАК и БАК): при химиотерапии – перед каждым циклом или каждые 2-3 недели;
- Капецитабин: периодически ЭКГ;
- Тамоксифен: ежегодный гинекологический осмотр; периодически ОАК и БАК (включая уровень кальция);
- Летрозол, Анастрозол, Эксеместан: ежегодная денситометрия;
- Сунитиниб, Сорафениб, Пазопаниб, Акситиниб: ежедневное измерение АД; ОАК, БАК, ОАМ перед каждым циклом или каждые 2-3 недели; периодически ЭКГ; ЭхоКГ каждые 12-24 недели;
- Регорафениб: обязательно АЛТ и АСТ не реже 1 раза в месяц, периодически ОАК и БАК, контроль АД, периодически ЭКГ;
- Гефитиниб, Эрлотиниб: периодически оценка печеночной функции (АЛТ, АСТ, общий билирубин);
- Афатиниб: периодически оценка печеночной функции (АЛТ, АСТ, общий билирубин), ЭхоКГ (ФВЛЖ) и осмотр офтальмолога;
- Осимертиниб: периодически оценка печеночной функции (АЛТ, АСТ, общий билирубин), ЭКГ (интервал QT) и осмотр офтальмолога;
- Кризотиниб: периодически ОАК, оценка печеночной функции (АЛТ, АСТ, общий билирубин), ЭКГ (интервал QT) и осмотр офтальмолога;
- Олапариб: ежемесячно ОАК;
- Палбоциклиб: ОАК перед каждым циклом;
- Рибоциклиб: ОАК, АЛТ и АСТ перед каждым циклом, периодически ЭКГ, контроль электролитов (калия, кальция, фосфатов и магния) первые 6 циклов;
- Лапатиниб: ЭхоКГ (контроль ФВЛЖ), контроль показателей функции печени (АЛТ, АСТ, общего билирубина и ЩФ) до начала терапии, далее каждые 4–6 недель;
- Дабрафениб: креатинин после лихорадки, ЭКГ до лечения, через 1 месяц после начала лечения и после изменения дозы, контроль глюкозы при СД, осмотр кожных покровов;
- Траметиниб: креатинин после лихорадки, периодически ЭхоКГ (ФВЛЖ), контроль АД, осмотр офтальмолога при симптомах нарушения зрения, контроль функции печени каждые 4 недели в течение 6 месяцев после начала лечения, осмотр кожных покровов;
- Вемурафениб: ЭКГ и контроль электролитов 1 раз в месяц, осмотр офтальмолога, осмотр кожных покровов, контроль функции печени каждые 4 недель;
- Кобиметиниб: осмотр офтальмолога, контроль ЭхоКГ (ФВЛЖ) каждые 3 месяца, контроль функции печени, креатинина и КФК каждые 4 недели.
Заключение
- Пероральная противоопухолевая терапия – это терапия в форме таблеток или капсул.
- Это удобно (повышается социальная активность пациента, поскольку больше не требуется постоянное пребывание в больнице). Появляется все больше пероральных противоопухолевых препаратов.
- Пероральная противоопухолевая лекарственная терапия показана не для всех типов рака.
- Нужна ответственность со стороны пациента: не пропускать приемы лекарства, следить за состоянием своего здоровья.
- Необходимо наличие возможности связи с лечащим врачом при появлении осложнений.
Источники:
- Каприн А.Д., Старинский В.В., Петрова Г.В. Злокачественные новообразования в России в 2018 году (заболеваемость и смертность). Москва: МНИОИ им. П.А. Герцена филиал ФГБУ «НМИЦ радиологии» Минздрава России, 2019. 250 p.
- Руководство по химиотерапии опухолевых заболеваний. 4th ed. / ed. Переводчикова Н.И., Горбунова В.А. Москва: Практическая медицина, 2018. 688 p.
- Regan M.M. Predicting Benefit of Endocrine Therapy for Early Breast Cancer // Breast. 2015. Vol. 24, № 0 2. P. S129–S131.
- Luo H.Y. et al. Single-agent capecitabine as maintenance therapy after induction of XELOX (or FOLFOX) in first-line treatment of metastatic colorectal cancer: randomized clinical trial of efficacy and safety // Ann. Oncol. 2016. Vol. 27, № 6. P. 1074–1081.
- Клинические рекомендации: Рак молочной железы. Общероссийский национальный союз “Ассоциация онкологов России.” 2020.
- Клинические рекомендации: Рак ободочной кишки. Общероссийский национальный союз “Ассоциация онкологов России.” 2020.
- Клинические рекомендации: Рак прямой кишки. Общероссийский национальный союз “Ассоциация онкологов России.” 2020.
- Клинические рекомендации: Рак яичников/рак маточной трубы/первичный рак брюшины. Общероссийский национальный союз “Ассоциация онкологов России.” 2020.
- Клинические рекомендации: Рак тела матки и саркомы матки. Общероссийский национальный союз “Ассоциация онкологов России.” 2020.
- Клинические рекомендации: Рак шейки матки. Общероссийский национальный союз “Ассоциация онкологов России.” 2020.
- Клинические рекомендации: Злокачественное новообразование бронхов и легкого. Общероссийский национальный союз “Ассоциация онкологов России.” 2020.
- Клинические рекомендации: Рак паренхимы почки. Общероссийский национальный союз “Ассоциация онкологов России.” 2020.
- Клинические рекомендации: Меланома кожи и слизистых оболочек. Общероссийский национальный союз “Ассоциация онкологов России.” 2020.
- Chon S.Y. et al. Chemotherapy-induced alopecia // J. Am. Acad. Dermatol. 2012. Vol. 67, № 1. P. e37-47.
- Aapro M. et al. MASCC/ESMO Antiemetic Guideline 2016 With Updates in 2019. Multinational Association of Supportive Care in Cancer. 2019. P. 55.
- Blum J.L. et al. Multicenter phase II study of capecitabine in paclitaxel-refractory metastatic breast cancer // J. Clin. Oncol. 1999. Vol. 17, № 2. P. 485–493.
- Bhojani N. et al. Toxicities associated with the administration of sorafenib, sunitinib, and temsirolimus and their management in patients with metastatic renal cell carcinoma // Eur. Urol. 2008. Vol. 53, № 5. P. 917–930.
- Тамоксифен (Tamoxifen®) — инструкция по применению, состав, аналоги препарата, дозировки, побочные действия [Electronic resource]. URL: https://www.rlsnet.ru/tn_index_id_3077.htm#pobochnye-dejstviya (accessed: 27.07.2020).
- Эндоксан® (Endoxan®) — инструкция по применению, состав, аналоги препарата, дозировки, побочные действия [Electronic resource]. URL: https://www.rlsnet.ru/tn_index_id_3690.htm (accessed: 27.07.2020).